En el examen final, la vacuna de Pfizer elevó al 95% su efectividad contra el coronavirus

La farmacéutica estadounidense Pfizer anunció este miércoles que su vacuna contra el coronavirus mostró una efectividad del 95% en un análisis final y sin problemas de seguridad.
La semana pasada, la empresa informó que su investigación, en conjunto con la firma BioNTech, había logrado 90% de efectividad, según el primer análisis intermedio de su ensayo de fase 3, la última etapa antes de pedir formalmente su homologación.
«La eficacia fue constante en los datos demográficos de edad, raza y etnia. La eficacia observada en adultos mayores de 65 años fue superior al 94%”, afirmaron Pfizer y su socio alemán BioNTech en un comunicado conjunto.
Las empresas explicaron que contaron 170 casos de infección por coronavirus entre los voluntarios que participaron en el ensayo: 162 infecciones ocurrieron en personas que recibieron placebo o inyecciones de solución salina, mientras que ocho casos fueron en participantes que recibieron dos dosis de la vacuna real. «Eso resulta en una eficacia del 95%,», aseguraron.
«Se observaron 10 casos graves de covid-19 en el ensayo, nueve de los cuales ocurrieron en el grupo de placebo y uno en el grupo vacunado con BNT162b2 (nombre experimental de la vacuna)», añade el comunicado.
Otro dato clave del análisis final realizado por Pfizer es que no se reportó ningún problema de seguridad grave relacionado a la vacuna. El análisis demuestra que la vacuna fue bien tolerada y que la mayoría de los eventos adversos solicitados se resolvieron poco después de la vacunación.
BREAKING: We are proud to announce, along with @BioNTech_Group, that the Phase 3 study of our #COVID19 vaccine candidate has met all primary efficacy endpoints.
— Pfizer Inc. (@pfizer) November 18, 2020
«Los únicos eventos adversos solicitados de Grado 3 (graves) mayores o iguales al 2% en frecuencia después de la primera o segunda dosis fueron fatiga al 3.8% y dolor de cabeza al 2.0% después de la dosis 2. De acuerdo con los resultados compartidos anteriormente, los adultos mayores tendían a informar menos eventos adversos solicitados y más leves después de la vacunación», detalla el informe.
Además, las empresas anunciaron que se logró el mínimo de seguridad requerido por la Administración de Drogas y Alimentos de los EE. UU. (FDA) para la Autorización de uso de emergencia (EUA), por lo que Pfizer y BioNTech planean enviar una solicitud de autorización. Los datos también se enviarán a otras agencias reguladoras de todo el mundo.
La protección rápida que brinda esta vacuna, combinada con su perfil de tolerancia en todos los grupos de edad estudiados hasta ahora, debería ayudar a hacer de esta vacuna una herramienta importante para abordar la pandemia actual”, dijo el Dr. Ugur Sahin, director ejecutivo y cofundador de BioNTech.
Argentina forma parte de los países en los que se llevan adelante las pruebas de la vacuna de Pfizer. Unos 4500 voluntarios recibieron las dos dosis y fue fue «muy bien tolerada por todos los participantes».
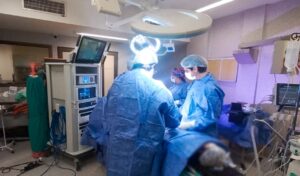
Pfizer avanza en el desarrollo de su vacuna.
El martes, el consejero delegado de la empresa, Albert Bourla, adelantó que la farmacéutica se encaminaba a pedir «de manera inminente» la autorización para su vacuna contra el Covid-19.
Cuando dieron a conocer el éxito de sus ensayos, Pfizer y BioNTech anunciaron que esperan producir 50 millones de dosis este año y 1.300 millones de dosis en 2021.
Además de Pfizer, otras potenciales de vacuna contra el coronavirus se encuentran en fase 3 y con resultados más que optimistas. El lunes, fue Moderna la que anunció una efectividad del 94,5%.
También la Sputnik V de Rusia mostró 92% de eficacia, vacuna de la que Argentina ya acordó con el gobierno de Vladimir Putin la compra de 25 millones de dosis, lo que alcanzaría para vacunar a 12,5 millones de personas, ya que requiere de dos aplicaciones.
China, en tanto, tiene varios desarrollos avanzados, aunque aún ninguno fue aprobado oficialmente por organismos internacionales.
Fuente: Clarín